 |
图1. 长非编码RNA NKILA调控不同亚群T细胞凋亡敏感性的机制
在国家自然科学基金项目(项目编号:81720108029,81622036, 81672614,81621004,81490750)等资助下,中山大学宋尔卫教授及苏士成副教授课题组揭示了LncRNA通过调控T细胞亚群的凋亡敏感性,从而改变肿瘤微环境中T细胞亚群的平衡,造成肿瘤免疫逃逸的新机制。研究成果以“NKILA LncRNA Promotes Tumor Immune Evasion by Sensitizing T Cells to Activation-induced Cell Death”(长链非编码RNA NKILA通过调控T细胞的凋亡敏感性促进肿瘤免疫逃逸)为题,于2018年9月17日在Nature Immunology(《自然·免疫学》)上在线发表。宋尔卫、苏士成为文章的共同通讯作者,中山大学黄迪博士为第一作者,中山大学为唯一作者单位。论文链接: https://www.nature.com/articles/s41590-018-0207-y。
肿瘤免疫是机体对肿瘤细胞产生的特异性免疫反应。免疫系统通过识别肿瘤特异性抗原并递呈给T细胞,T细胞特异地清除这些“非正常”细胞,抵御肿瘤的发生发展。近年来,肿瘤免疫治疗取得了重大的突破,针对免疫检查点的抗体治疗、以及CAR-T为代表的细胞过继治疗等越来越多的免疫治疗方法获得了FDA突破性疗法资格。肿瘤免疫治疗能够在患者中产生持久抗肿瘤免疫记忆,即便治疗停止,仍然具有长期的保护作用,与其他传统的肿瘤治疗手段相比更具优势。
目前,免疫治疗的效果受限于肿瘤免疫逃逸。肿瘤免疫逃逸是指肿瘤细胞通过自身或微环境的改变,从而逃避免疫系统识别和攻击。肿瘤微环境的复杂网络显著地削弱了免疫治疗的功效,使免疫治疗在实体瘤中的开展仍有很大困难。促进肿瘤免疫逃逸的微环境有一个重要的特点:免疫抑制T细胞(Treg, TH2)富集,而抗肿瘤T细胞(CTL, TH1)缺乏。既往的研究多聚焦于肿瘤微环境使幼稚T细胞更多地分化为免疫抑制T细胞,或者免疫抑制T细胞的募集和增殖远高于抗肿瘤的T细胞。除此之外,是否还存在其他的调控机制尚未完全明确。
该课题组研究发现,在乳腺癌、肺癌的临床标本中,浸润的抗肿瘤T细胞(CTL, TH1)大部分处于凋亡状态,而免疫抑制T细胞(Treg, TH2)的凋亡极少。同时证明,尽管不同T细胞亚群Fas受体的表达量并无明显差异,抗肿瘤T细胞(CTL, TH1)在体外易被FasL诱导凋亡,而免疫抑制T细胞(Treg, TH2)则不易被FasL诱导凋亡,从而揭示了抗肿瘤T细胞(CTL, TH1)、免疫抑制T细胞(Treg, TH2)对肿瘤微环境中的FasL凋亡信号的反应性差异是导致肿瘤免疫逃逸的新机制。通过对比不同T细胞亚群的LncRNA表达谱,发现NKILA在凋亡敏感的T细胞中明显高表达,而沉默NKILA可使凋亡减少,杀伤功能明显增加。同样,NKILA在凋亡敏感的TH1中高表达,在凋亡耐受的Treg和TH2中低表达,介导了不同T细胞亚群的凋亡敏感性。进一步探索其机制,发现NKILA的转录受IFNγ-STAT1通路及TCR-钙调素信号通路共同调控,TCR-钙调素信号将结合于NKILA启动子的HDAC移除,便于CTL/TH1相关转录因子STAT1进入呈“开放”状态的启动子区,从而上调NKILA;NKILA通过遮挡IκBα的磷酸化位点,抑制NF-κB通路及下游抗凋亡基因转录,使CTL及TH1容易被诱导凋亡。
该研究选用了人源肿瘤异种移植(Patient-derived xenograft, PDX)模型,模拟人的过继性免疫治疗的过程,将修饰后的同源T细胞及树突状细胞回输至荷瘤小鼠体内。发现沉默NKILA的T细胞在荷瘤小鼠中的凋亡明显减少,可更多地浸润到肿瘤局部,行使杀伤功能,使肿瘤明显缩小。从而提示,TCR-T或者CAR-T细胞治疗在实体瘤中疗效不佳的原因,除已知的不能够有效地浸润到肿瘤组织内部等原因外,另一个重要的原因可能就是,在接触肿瘤之前,这类细胞就已经死于微环境中FasL等凋亡信号的调控。
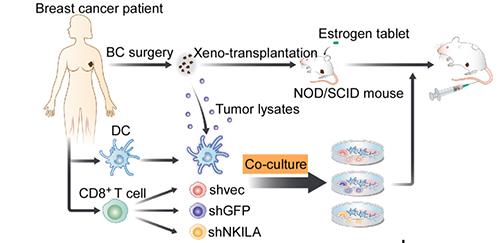
图2. 过继性回输沉默NKILA的T细胞在临床前PDX模型中显示疗效
该研究首次发现LncRNA通过调控T细胞亚群的凋亡敏感性,从而改变肿瘤微环境中免疫激活及免疫抑制的T细胞亚群的平衡,造成肿瘤的免疫逃逸,揭示了不同亚群T细胞凋亡敏感性存在差异的调控机制。提示,通过靶向NKILA LncRNA,能够保护T细胞顺利识别肿瘤细胞,从而为过继细胞免疫治疗提供了新的思路。